Перевірка фейків у рамках партнерства з Facebook
У мережі поширюють відео з фейком про небезпеку медичного препарату «Парацетамол», який застосовують для хворих на COVID-19 як жарознижуючий препарат.
На відеозаписі голоси людей застерігають від вживання нібито отруєного парацетамолу, виробленого в Ізраїлі для поширення на території Палестини. У відео говорять, що препарат поширився на території Росії та Казахстану, й стверджують, що впродовж 5 днів після вживання цього ізраїльського парацетамолу людина помирає.
Незалежні литовські фактчекери з Patikrinta 15min вже спростовували подібний фейк ще у 2019 році.
Світлину з блістером таблеток, яку використовують у відео, помітили в соціальних мережах ще 2017 року. Тоді у фейку зазначали, що в цьому препараті заховали вірус Мачупо або ж вірус «чорного тифу». Тоді посадовці міністерства охорони здоров’я Малайзії офіційно спростовували небезпеку цього препарату, оскільки фейк стосувався переважно Малайзії й Сингапуру.
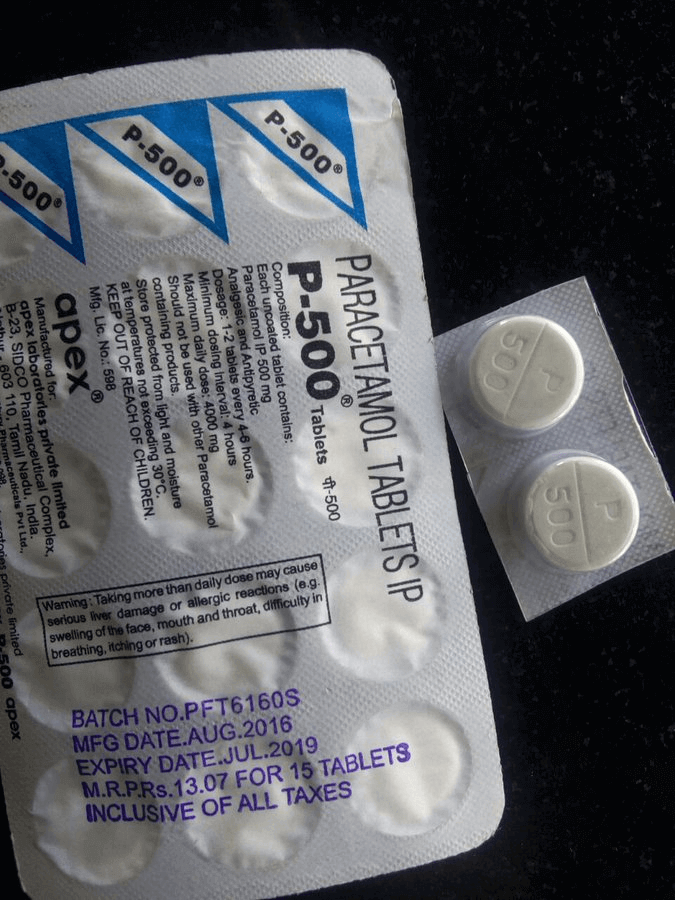
Утім, препарат навіть не вироблений в Ізраїлі. Угорі упаковки на світлині видно, що виробник препарату – індійська фармацевтична компанія «Apex». На їхньому сайті є сторінка цього препарату.
До того ж, якщо придивитись до написів на упаковці з оригінальної світлини, можна побачити, що препарат вироблено в серпні 2016 року, а строк придатності – липень 2019 року. Так, термін придатності препарату сплив ще до початку пандемії, і автори фейку просто взяли світлину з Інтернету, яку вже використовували для створення подібних фейків.
У Державному реєстрі лікарських засобів України немає ліцензії для медичного препарату «Парацетамол», виготовленого цією компанією та з таким маркуванням. Тобто, саме такий «Парацетамол», як у фейку, неможливо придбати в аптеках на території України. Відкликання медичного препарату при появі неконтрольованих дефектів чи побічних реакцій у пацієнтів регулюється 99 пунктом цих Ліцензійних умов.
Застереження
Автори не є співробітниками, не консультують, не володіють акціями та не отримують фінансування від жодної компанії чи організації, яка б мала користь від цієї статті, а також жодним чином з ними не пов’язаний



