Проверка фейков в рамках партнерства с Facebook
Пользователи соцсетей распространяют публикации о том, что в Украине продолжается так называемый «клинический эксперимент» — вакцинация от COVID-19. К примеру, в Facebook распространяют видео, на котором закадровый женский голос рассказывает, в каких официальных документах это указано. Автор ссылается на многочисленные законы и подзаконные нормативно правовые акты. Однако она ошибочно, по своему усмотрению трактует все официальные документы, вырывает из контекста отдельные фразы, а также ссылается на законы и постановления, не имеющие ничего общего с вакцинацией.
VoxCheck опровергает некоторые ложные утверждения из этого видео.
Ошибочный тезис: в Государственном реестре лекарственных средств препараты, называемые вакцинами от COVID-19, не имеют статуса вакцины. «Вакцины от COVID-19» – это торговое название. По документам это иммунологические препараты для экстренного использования.
Все доступные в Украине вакцины зарегистрированы и имеют статус вакцины.
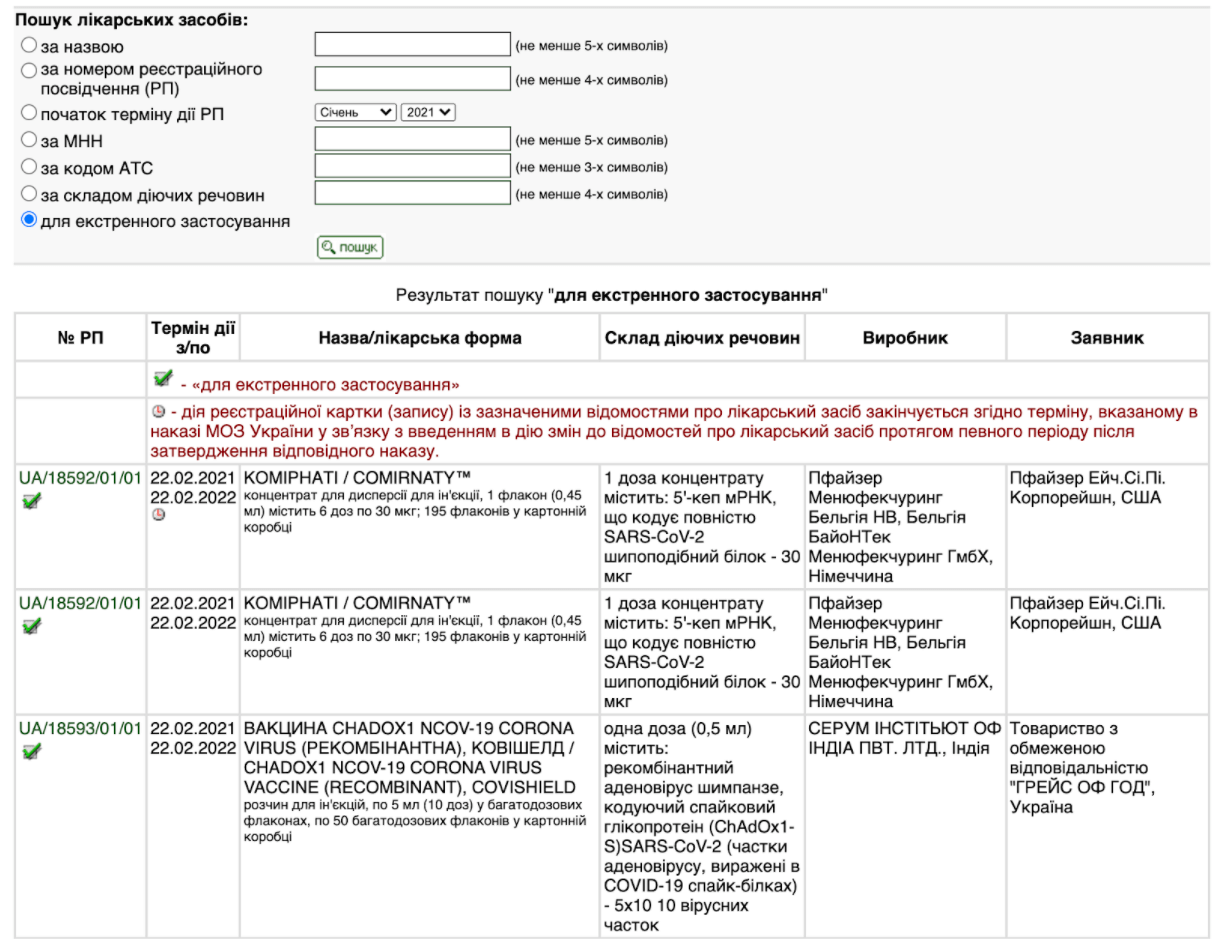
Во-первых, вакцины и являются иммунобиологическими препаратами, потому они так и зарегистрированы. Во-вторых, все вакцины, одобренные Минздравом, с соответствующей ссылкой на приказы можно найти на сайте Государственного реестра лекарственных средств, добавив фильтр «для экстренного применения». Общее название «вакцины от COVID-19» не является торговым названием. В то же время торговым названием/маркой являются Comirnaty, Covishield, Vaxzevria, Janssen, Coronavac – именно под такими названиями продают вакцины разработки Pfizer-BioNTech, Oxford-AstraZeneca, Sinovac Biotech, Johnson & Johnson.
Скриншот — Госреестр лекарственных средств
Там также указан состав действующих веществ каждой вакцины: аденовирус 26-го типа, кодирующий спаечный гликопротеин SARS-CoV-2, или инактивированный SARS-CoV-2 антиген, или мРНК, кодирующий полностью SARS-CoV-2 и т.д.
В-третьих, в соответствии с постановлением Кабинета Министров Украины № 95 от 08.02.2021, предусматривающим регистрацию вакцин для профилактики COVID-19 под обязательства для экстренного медицинского применения, вакцины производителя Pfizer (Cominarity), Johnson & Johnson (Janssen), Oxford /AstraZeneca (Covishield, AstraZeneca), Sinovac Biotech (CoronaVac) зарегистрированы в Украине и имеют статус вакцины. Только вакцина производителя Moderna (Spikevax) не зарегистрирована на территории Украины, она была получена в рамках международной инициативы COVAX.
Ошибочный тезис: По «золотому стандарту» клинических испытаний требуется не менее 5 лет для разработки безопасной вакцины. Сейчас идет всего 4 стадия клинического эксперимента.
Золотым стандартом клинических испытаний является двойное рандомизированное слепое исследование с использованием группы плацебо-контроля, а не срок, за который лекарственный препарат проходит 4 этапа клинического испытания. Разным препаратам требуется разный срок для прохождения всех стадий.
Вакцине, безусловно, важно пройти все этапы исследования. Но четвертый этап клинических испытаний и происходит уже после регистрации препарата. Все вакцины, которые используются в Украине, находятся на третьем этапе клинических испытаний.
Процесс разработки, проведение различных этапов клинических исследований, утверждение вакцин может длиться от 10 до 15 лет. В случае с вакциной против COVID-19 процесс длился 11 месяцев.
Вакцины от COVID-19 были столь быстро утверждены для экстренного применения в связи со многими факторами. Во-первых, SARS-CoV-2 – не первый вирус в истории семейства коронавирусов и у ученых уже были определенные предварительные наработки. Во-вторых, правительства стран мира выделили большие средства для разработки этих вакцин. В-третьих, учёные со всего мира сотрудничали.
Вакцины, которыми проводят прививку в Украине, прошли этапы клинических испытаний, доказывающие безопасность и эффективность.
Компании Pfizer и BioNTech (США и Германия) в промежуточном отчете третьего этапа испытаний заявили о 90% эффективности. На этом этапе клинических испытаний приняло участие более 40 тыс. волонтеров. В ноябре 2020 года Moderna в промежуточном отчете третьего этапа заявила о 95% эффективности своей вакцины, на этом этапе приняли участие более 30 тыс. волонтеров.
Промежуточные результаты испытаний AstraZeneca показали, что вакцина на 79% эффективна в предотвращении симптоматического течения COVID-19 и на 100% защищает от тяжелого течения болезни и госпитализации. Промежуточные результаты третьей фазы испытаний вакцины CoronaVac были опубликованы в июле 2021 года. Они показали, что CoronaVac обеспечивает 83,5% защиту от симптоматического COVID-19.
Ошибочный тезис: То, что вакцинация — это «клинический эксперимент», доказывает приказ Минздрава №1775
Приказ Минздрава Украины от 20.08.2021 №1775, на который ссылается автор, нет ничего общего с вакцинацией, поскольку в нем говорится об испытаниях препарата «PF-07321332/ритонавир». Автор манипулирует названием компании — «Пфайзер Инк.», которая производит вакцину Comirnaty и отдельно разрабатывает новый таблетированный препарат, о котором идет речь в приказе №1775. К тому же это не может быть массовой вакцинацией, потому что испытания таблеток проходили всего в 8 украинских больницах.
В начале ноября в Pfizer сообщили, что по результатам клинического испытания ритонавир снижает риск госпитализации или смерти на 86% по сравнению с плацебо у негоспитализированных взрослых с высоким риском заболеть COVID-19. Если дальнейшие результаты дальнейших клинических испытаний будут успешными и препарат зарегистрируют в США или ЕС, Украина будет закупать ритонавир. На брифинге 16 декабря Виктор Ляшко сообщил, что Украина подписала договор с компанией Pfizer на закупку препарата «Паксловид» — именно под этим названием продают ритонавир.
Кроме этого автор утверждает, что так называемый «эксперимент» запланировали Законом Украины 2362-VIII «О внесении изменений в некоторые законы Украины относительно полномочий в области охраны окружающей природной среды». Этот фейк мы уже опровергали раньше.
В сети также распространяют два скриншота, которые якобы доказывают проведение в Украине «клинического эксперимента». На эти же документы ссылаются в упомянутом видео.
Скриншоты из публикаций в Facebook
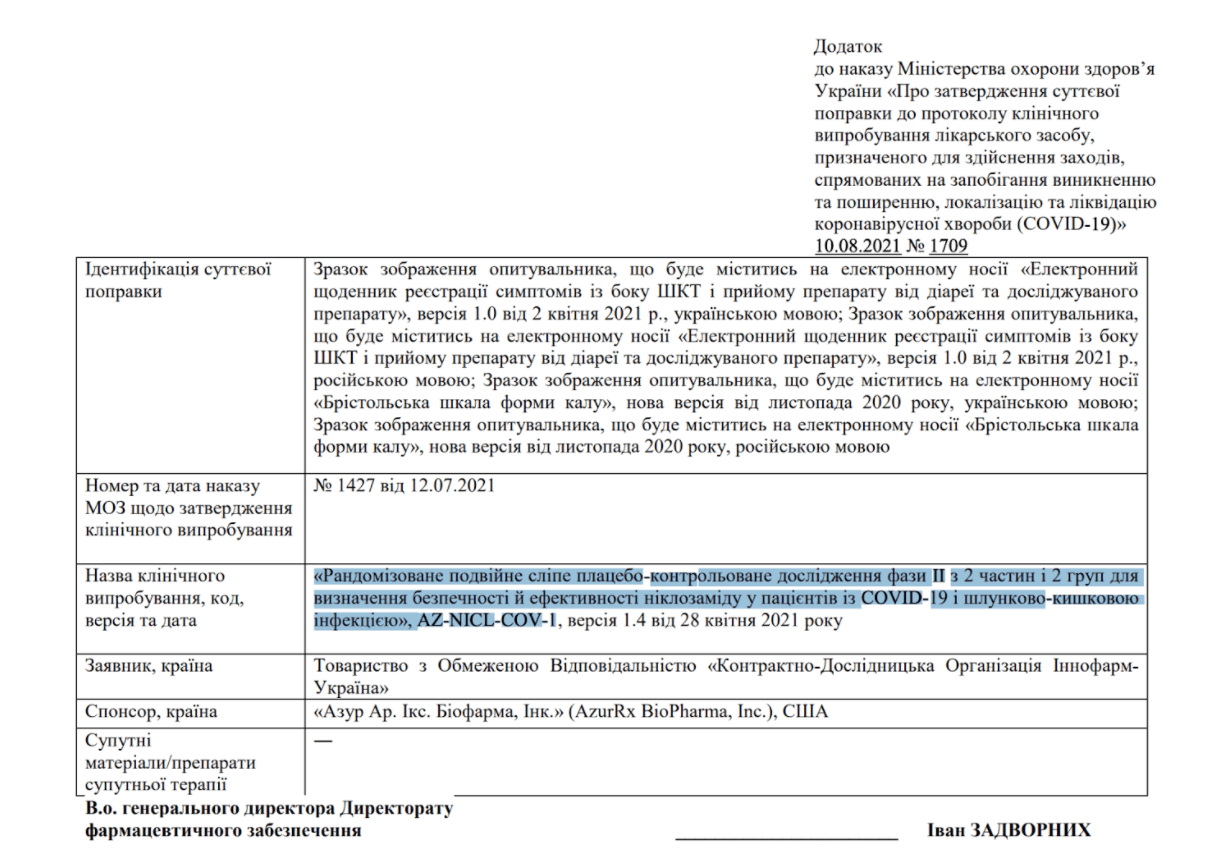
Однако в упомянутых приказах речь не идет о «клиническом эксперименте», а о клинических испытаниях отдельных препаратов — даже не вакцин от COVID-19. Например, в приложении к приказу №1709 указано, что будут испытывать препарат никлазамид у пациентов с COVID-19 и желудочно-кишечной инфекцией.
Приложение к приказу Минздрава №1709
В приказе №1553 речь идет об испытаниях терапии для пациентов с раком легких, а не вакцины или лекарства от COVID-19.
Приложение к приказу Минздрава №1553
Предостережение
Авторы не работают, не консультируют, не владеют акциями и не получают финансирования от компании или организации, которая бы имела пользу от этой статьи, а также никоим образом с ними не связаны